Covid-19: por qué las primeras vacunas exigen congelación
Noviembre ha traído noticias optimistas sobre las vacunas que están produciendo las empresas de biotecnología Moderna y Pfizer/BioNTech. Ambas utilizan una tecnología nueva, la del ARN mensajero (ARNm). Al tratarse de moléculas lábiles, se enfrentan al mismo desafío: deben almacenarse a temperaturas muy frías.
Recordemos que las más de 180 candidatas a vacunas contra el SARS-CoV-2 están basadas en diferentes plataformas de síntesis (Figura 1). Unas optaron por usar virus SARS-CoV-2 completos inactivados que no pueden multiplicarse. Otras decidieron usar la técnica de vectores con virus no-replicativos: el virus se modifica genéticamente para reducir su virulencia e impedir que se replique. Estos tipos de vacunas, que siguen el modelo clásico, son las más comunes y se usan para desarrollar las dosis contra la gripe, el sarampión o el ébola.
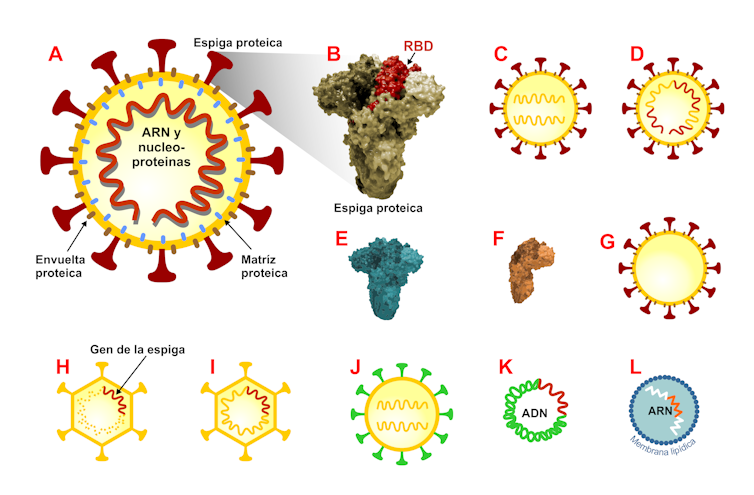 Las vacunas en proceso están basadas en varias plataformas diferentes que se pueden dividir en: a) enfoques tradicionales (vacunas inactivadas o con virus vivos); b) plataformas que han dado lugar a vacunas autorizadas recientemente (vacunas de proteínas recombinantes y vacunas vectorizadas), y c) vacunas de ARN y de ADN). A, Esquema de las proteínas estructurales del virión del SARS-CoV-2 (véase a mayor detalle en la Figura 2). B, Estructura de la espiga proteica espiculada: un monómero se resalta en marrón oscuro y el dominio de unión al receptor (RBD) en rojo. C-l, las vacunas candidatas actuales incluyen: de virus inactivados (C), vivas atenuadas (D), de proteínas recombinantes basadas en la espiga proteica (E), basadas en el RBD (F) o en partículas similares a virus (G), de vector de replicación incompetente (H), de vector de replicación competente (I), de vector de virus inactivado que muestran la espiga proteica en superficie (J), de ADN (K), y de ARN (L). Modificada a partir de F. Krammer (Nature, 586: 516-527; 2020). Imagen facilitada por Luis Monje.
Las vacunas en proceso están basadas en varias plataformas diferentes que se pueden dividir en: a) enfoques tradicionales (vacunas inactivadas o con virus vivos); b) plataformas que han dado lugar a vacunas autorizadas recientemente (vacunas de proteínas recombinantes y vacunas vectorizadas), y c) vacunas de ARN y de ADN). A, Esquema de las proteínas estructurales del virión del SARS-CoV-2 (véase a mayor detalle en la Figura 2). B, Estructura de la espiga proteica espiculada: un monómero se resalta en marrón oscuro y el dominio de unión al receptor (RBD) en rojo. C-l, las vacunas candidatas actuales incluyen: de virus inactivados (C), vivas atenuadas (D), de proteínas recombinantes basadas en la espiga proteica (E), basadas en el RBD (F) o en partículas similares a virus (G), de vector de replicación incompetente (H), de vector de replicación competente (I), de vector de virus inactivado que muestran la espiga proteica en superficie (J), de ADN (K), y de ARN (L). Modificada a partir de F. Krammer (Nature, 586: 516-527; 2020). Imagen facilitada por Luis Monje.Por su parte, Moderna y Pfizer/BioNTech han ensayado y puesto a punto un tipo de vacuna inédito que utiliza un fragmento pequeño del ARN mensajero del virus (ARNm) para convertir las células de un paciente en fábricas que producen una proteína del coronavirus, concretamente la que forma las espigas con las que el virus penetra en nuestras células.
La secuencia de ARNm vírico inyectada mediante la vacuna no basta para causar el daño que haría un virus completo, pero es suficiente para que nuestro sistema inmunológico aprenda a reconocerla y sea capaz de desatar una respuesta inmune para combatir futuras infecciones. Al detectar la secuencia de la proteína espiculada, nuestro sistema inmunológico produce anticuerpos y estimula a las células T, los linfocitos producidos en el timo cuyo principal propósito es identificar y destruir a las células infectadas.
La construcción de la vacuna
Piense en la vacuna como en una onza de chocolate que se derrite fácilmente a temperatura ambiente. Así como hay formas de evitar que el chocolate se derrita, los biotecnólogos de ambas compañías farmacéuticas idearon mecanismos para proteger sus ensayos. Dada la promiscuidad reactiva de algunas biomoléculas, protegerlas no resulta sencillo.
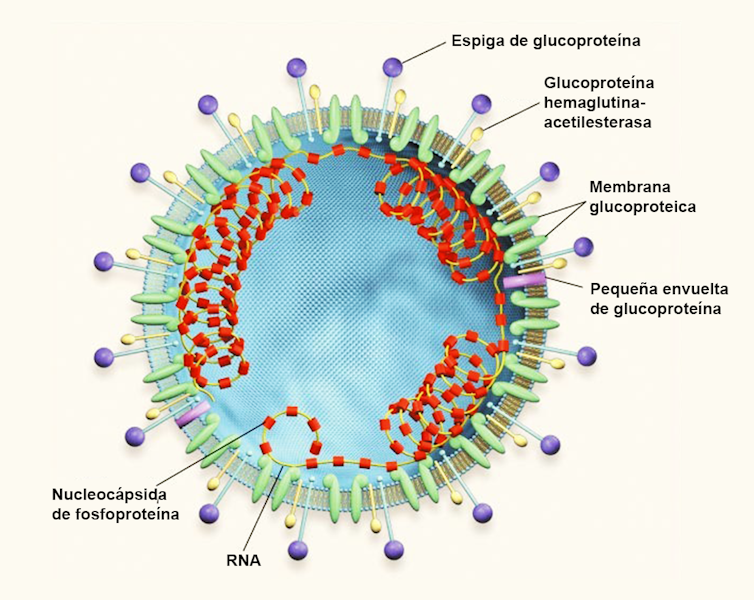 Figura 2. Estructura típica del virión de un coronavirus de tipo 2. El genoma del ARN y la fosfoproteína de la nucleocápside viral forman una nucleocápside helicoidal. Una corona de picos grandes y distintivos en la envoltura permite identificar a los coronavirus por microscopía electrónica. Los picos, oligómeros de la glucoproteína pico (S), se unen a los receptores de las células huésped y fusionan la envoltura viral con las membranas de la célula huésped. Los coronavirus del grupo 2 también tienen una glucoproteína hemaglutinina-acetilesterasa que se une a los restos de glucosa en las membranas celulares. Modificado a partir de K.V. Holmes (N Engl J Med 348:1948-1951; 2003). Luis Monje.
Figura 2. Estructura típica del virión de un coronavirus de tipo 2. El genoma del ARN y la fosfoproteína de la nucleocápside viral forman una nucleocápside helicoidal. Una corona de picos grandes y distintivos en la envoltura permite identificar a los coronavirus por microscopía electrónica. Los picos, oligómeros de la glucoproteína pico (S), se unen a los receptores de las células huésped y fusionan la envoltura viral con las membranas de la célula huésped. Los coronavirus del grupo 2 también tienen una glucoproteína hemaglutinina-acetilesterasa que se une a los restos de glucosa en las membranas celulares. Modificado a partir de K.V. Holmes (N Engl J Med 348:1948-1951; 2003). Luis Monje.Las reacciones orgánicas obedecen ciegamente (si no lo hacen, las cosas irán muy mal) a los genes. Lo que hacen los genes es dar instrucciones para fabricar proteínas. La mayoría de las cosas útiles que hay en el cuerpo lo son. Algunas, las hormonas, transmiten mensajes químicos. Otras, los anticuerpos, atacan a los agentes patógenos. Otras proteínas, las enzimas, son catalizadores que aceleran una reacción orgánica disminuyendo la energía de activación o cambiando el mecanismo de reacción.
El problema para los biotecnólogos que trabajan con ARN es que se trata de una molécula bajo la amenaza constante de ser destruida por las ribonucleasas (ARNasas), las enzimas que catalizan la hidrólisis del ARN fragmentando su cadena de ribonucleótidos en componentes más pequeños. Dicho de otra forma: descomponen el rompecabezas genético del virus desarmando sus piezas.
Las ribonucleasas constituyen una línea de defensa primaria contra los agentes infecciosos que utilizan ARN como información genética y por eso son extremadamente comunes, tan comunes que pueden estar en el aliento de un investigador, en su piel o en cualquier cosa que haya tocado, lo que trae como consecuencia que cualquier ARN tenga una vida muy corta en un ambiente desprotegido.
El mecanismo de protección que se usa en biotecnología es el inhibidor de la ribonucleasa (IR), que se une a ciertas ribonucleasas con mayor afinidad que cualquier otra interacción proteína-proteína, evitando que estas “ataquen” al ARN. La IR se usa en la mayoría de los laboratorios que estudian el ARN para proteger sus muestras de la degradación por parte de las ARNasas ambientales bajo condiciones de laboratorio.
Por eso, los biotecnólogos realizaron primero algunas modificaciones en la estructura molecular del ARNm para hacerlo más estable. Básicamente, lo que hicieron fue modificar los nucleótidos del ARNm (las “piezas del puzle” del genoma viral) utilizando versiones modificadas más estables. Eso es algo así como cambiar algunos ingredientes del chocolate para que no se derrita demasiado sin perder sus esencias.
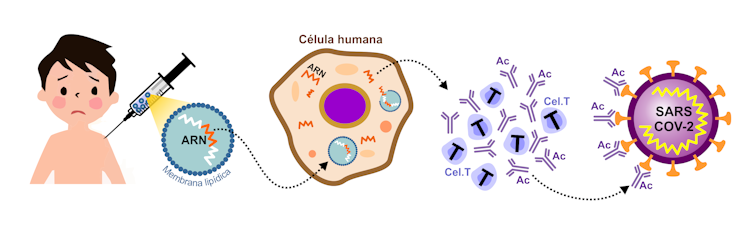 Figura 3. Cómo funciona una vacuna ARN. Los investigadores toman parte del ARN del virus y lo recubren con un lípido para que pueda introducirse en las células corporales mediante una inyección intramuscular. La vacuna ingresa en las células y el ARN les ordena que produzcan las proteínas de la espiga del coronavirus. Eso hace que el sistema inmunológico produzca anticuerpos (AC) y active las células T para destruir las células infectadas. Si el paciente tiene coronavirus, los anticuerpos y las células T se activan para combatirlo. Luis Monje.
Figura 3. Cómo funciona una vacuna ARN. Los investigadores toman parte del ARN del virus y lo recubren con un lípido para que pueda introducirse en las células corporales mediante una inyección intramuscular. La vacuna ingresa en las células y el ARN les ordena que produzcan las proteínas de la espiga del coronavirus. Eso hace que el sistema inmunológico produzca anticuerpos (AC) y active las células T para destruir las células infectadas. Si el paciente tiene coronavirus, los anticuerpos y las células T se activan para combatirlo. Luis Monje.El chocolate comercial, se presente en la forma que se presente, va inmerso en una receta que incluye estabilizantes y conservantes, entre otros aditivos cuyo uso es impensable en una vacuna. Por eso, para evitar cualquier daño, los investigadores no solo tienen que realizar cambios químicos en el ARNm y envolverlo en una capa protectora, también deben almacenarlo a bajas temperaturas hasta conseguir que las reacciones químicas se ralenticen hasta casi detenerse.
Pura química o, mejor dicho, pura cinética química. Las reacciones químicas tienen cinéticas diferentes, es decir, transcurren a diferentes velocidades. Por ejemplo, la oxidación del hierro bajo condiciones atmosféricas es una reacción lenta que puede tardar años para completarse, mientras que la combustión del gas natural es una reacción que sucede en fracciones de segundos.
Todo sucede más lentamente a medida que baja la temperatura. Por lo tanto, las reacciones químicas desatadas por las enzimas que descomponen el ARN se ralentizan. Es lo mismo que congelar los alimentos para evitar que se echen a perder.
¿Por qué se necesitan temperaturas tan bajas?
Además de su mecanismo de activación inmunológico, las dos vacunas pendientes de aprobación tienen algo en común. Una membrana de nanopartículas de lípidos rodea el ARNm, revistiéndolo con una especie de envoltura que podemos comparar con un Lacasito, una lenteja de chocolate dentro de una envuelta de caramelo que consigue que el chocolate no se derrita. En los diferentes lípidos utilizados por Moderna y Pfizer/BioNTech residen las diferencias de temperatura que necesita la conservación de sus respectivas vacunas.
A largo plazo, la vacuna de Moderna se puede almacenar a -20 ⁰C, mientras que la de Pfizer/BioNTech necesita congelarse a -70 ⁰C, una temperatura más fría que un invierno antártico. Ambas vacunas requieren que las personas reciban dos inyecciones, con tres semanas de diferencia. Eso significa duplicar los requisitos de capacidad, lo que representa una complicación adicional: los centros de salud, los hospitales y otros posibles sitios de vacunación necesitarán almacenar una gran cantidad de vacunas en sus instalaciones sin que se rompa la cadena de frío.
Es ahí donde reside el talón de Aquiles de la vacuna Pfizer/BioNTech, porque para conseguir su temperatura de conservación deberá usar ultracongeladores, que necesitan energía eléctrica, son caros y bastante voluminosos, o hielo seco, unos cilindros de CO₂ congelado que se pueden meter en una caja para transportar la vacuna y pueden durar una quincena si se cambia el hielo seco cada cinco días. En ese punto Moderna tiene ventaja, porque su vacuna dura seis meses a la temperatura que alcanzan los congeladores domésticos e incluso un mes en la cabina principal de un frigorífico.
No obstante, desde Covax, la alianza formada por más de 170 países para facilitar el acceso equitativo global a las vacunas, son optimistas frente al reto de almacenar las vacunas que requieren ultracongelación: la actual vacuna contra el ébola requiere un almacenamiento de entre -70° C y -80° C y, aun así, se han hecho vacunaciones masivas durante las recientes epidemias africanas.
Por lo demás, ya están en marcha los primeros ensayos de una vacuna “caliente”, es decir, termoestable. La ciencia no ha dicho la última palabra. Queda todavía mucho camino por recorrer.
Este artículo fue publicado originalmente en The Conversation. Lea el original.




































